人用药品注册技术要求国际协调会(ICH)作为全球药品监管协调的核心平台,已起草发布了多项技术指导原则,分为质量(Q)、安全性(S)、有效性(E)及综合类(M)4个系列,这些指导原则已成为代表国际标准的药品注册技术要求。
质量指导原则(ICH-Q部分)
ICH-Q部分指导原则,根据主题的不同,主要分为14个子类,在化学、生产与控制以及质量管理方面提供指导,14个子类指南分别为[1]:
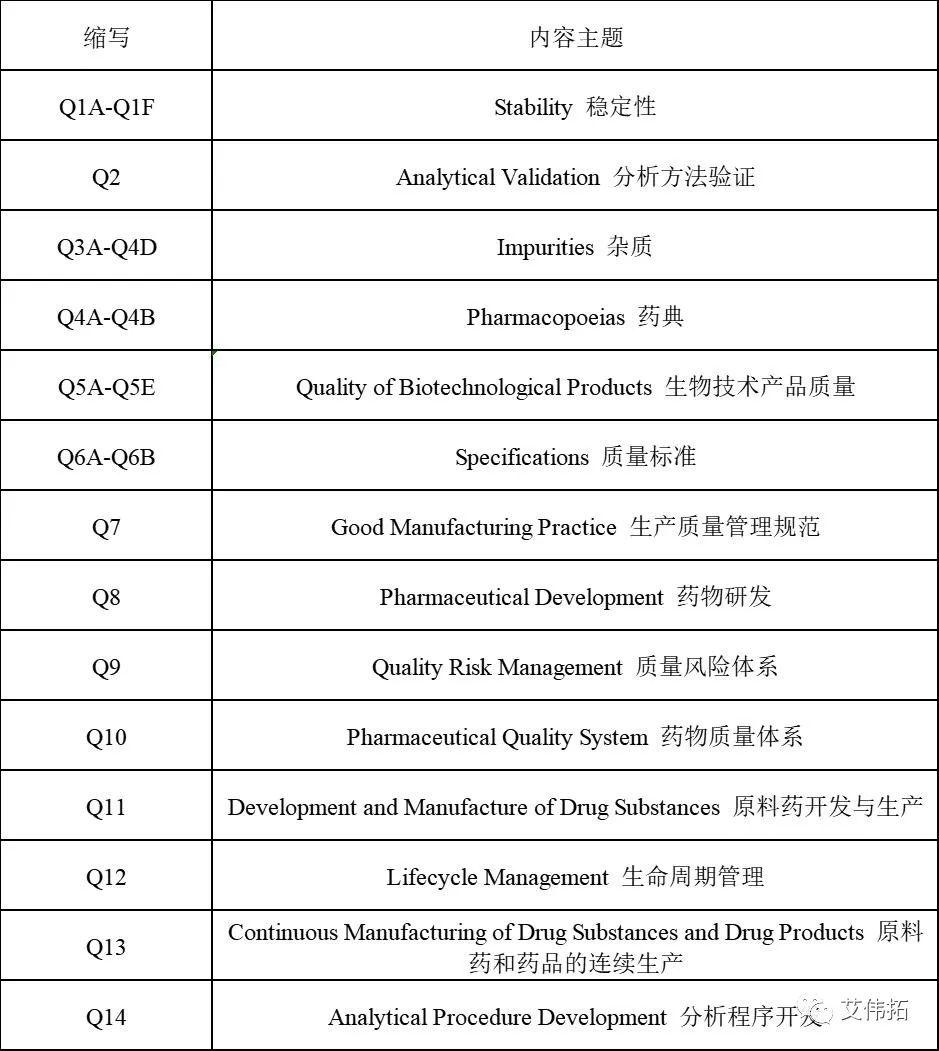
ICH Q1 Stability稳定性
稳定性试验的目的是考察原料药物或制剂在温度、湿度、光线的影响下随时间变化的规律,为药品的生产、包装、贮存、运输、使用等提供科学依据。
ICH Q1指南中共包括了7个指南文件,分别从不同角度阐述化合物的稳定性研究,包括Q1A-Q1F以及EWG针对ICH稳定性指南系列的修订说明Q1/Q5C。Q1A是ICH Q1系列指南文件的主体,阐述了稳定性研究的原理及目的,并分别对原料药和药品就批次选择与包装、质量标准、检测频率、储存条件、稳定性研究、标签等内容进行阐述,Q1B-Q1F从不同侧面对Q1A内容进行补充。
关于ICH Q类指导原则,可以去ICH官网ICH Official web site : ICH 进行查询,也可去药品审评中心(CDE)官网的指导原则专栏下的ICH指导原则ICH指导原则 (cde.org.cn)下载中文版ICH指导原则。
[1] ICH Official web site : ICH