一图看懂本文:
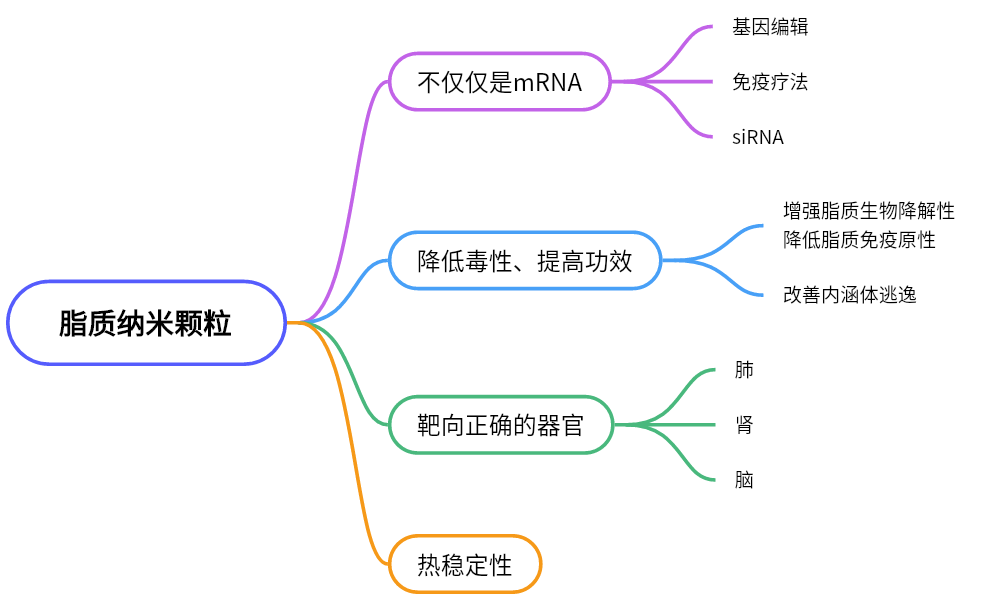
图1.**是mRNA-LNP主要适应症之一
Barbara Mui自1990年在Pieter Cullis课题组读博至今,一直在研究LNP及其前身Liposome。
Mui目前是Acuitas的高级科学家,该公司开发了BioNTech-Pfizer联合开发的mRNA**疫苗中所用的LNP脂质体。Mui说:“早期,LNP用于封装**药物,但随着研究的深入,LNP作为核苷酸的递送载体,效果更好。当然,**个取得非常好效果的LNP药物,是用于封装siRNA的。”
但事实证明,mRNA是***的载荷。LNP由带正电荷的脂质体纳米颗粒组成,这些颗粒封装带负电荷的mRNA。一旦进入体内,LNP通过内吞作用进入细胞,在完成内涵体逃逸后,释放到细胞质中。“如果没有专门设计的化学物质,LNP和mRNA将在内涵体中被降解,”卡内基梅隆大学,化学工程和生物医学工程系教授Kathryn Whitehead说。
LNP是mRNA的理想递送系统。“****加速了人们对LNP的接受和认知,人们对它们更感兴趣了,”Mui说。下一个可能是针对***毒或疟疾等其他传染病或**等非传染性疾病的LNP-mRNA疫苗。而且LNP的递送潜力并不止于mRNA,还有更大的空间来调整LNP来运输不同类型的载荷。但为了实现这些潜在的好处,研究人员首先需要克服挑战并降低毒性,提高他们从内涵体中逃逸的能力,增加他们的热稳定性,并研究如何有效地将LNP靶向全身**。
挑战1、超越mRNA
众所周知,LNP是递送mRNA***的载体之一,目前也是被人**研究。然后除了mRNA,LNP还可以在其他领域发挥作用。
基因编辑
“该领域目前*令人兴奋的方向是基因编辑,”EnterX Bio的科学家Yulia Eygeris说,EnterX Bio是一家由Eygeris的博士后主管Gaurav Sahay于2021年创立的公司,旨在将LNP研究商业化。EnterX Biosciences - Delivering the Future of Genetic Medicines
LNP可以携带Cas9 mRNA等基因编辑机制或引导RNA进入细胞。这为LNPs提供了用作基因**递送系统的能力。目前,临床试验中有一种基于LNP的CRISPR-Cas9候选**杂合子家族性高胆固醇血症患者,其靶向肝脏中的PCSK9基因。其他基因**的可能性可能包括操纵囊性纤维化患者的CFTR基因,或用于**罕见的遗传疾病。
免疫疗法
LNP的另一个潜在应用是免疫疗法。对淋巴细胞(如T细胞或NK细胞)进行基因修饰,并且经过证明,对血*是有用的。通常,该过程涉及从接受**的人的血液中提取淋巴细胞,编辑培养中的细胞以表达CAR,然后将其重新引入血液中。然而,LNP可以通过将CAR mRNA递送到靶淋巴细胞上,在体内表达所需的CAR。Mui参与了一项体内研究,表明在这一过程,LNP-mRNA在小鼠T细胞中发挥了作用(Rurik,J.G.et al,Science 375,91-96,2022)。ProMab Biotechnologies研发副总裁Vita Golubovskaya在CAR-TCR峰会上展示了关于将CAR-mRNA引导到NK细胞然后可以杀死靶细胞的LNP的初步数据。“RNA-LNP是一种非常令人兴奋和新颖的技术,可用于递送针对**的CAR和双特异性抗体,”她说。
siRNA
LNP还可以携带小的干扰RNA(siRNA),例如在patisiran中,这是FDA批准的**种siRNA药物,它使用LNPs递送siRNA来对抗称为甲状腺素转运蛋白的错误折叠。通过抑制转甲状腺素蛋白的产生来**淀粉样变性。
LNP仍然需要进行大量的研究,以在其所有不同的角色中充当**载体。主要挑战之一是基因**和其他常规**相比疫苗,需要更高的剂量或更多的**。在这些较高剂量下,LNPs会导致细胞毒性反应,因此降低LNPs的毒性是研究中的重中之重。
有不同的方法可以使LNP**的毒性降低。一种是通过研究脂质体如何影响毒性。
“如果脂质体完全可降解,就有解决方案,”特拉维夫大学纳米医学实验室主任Dan Peer说。在递送完API之后,徘徊在细胞中的脂质体比那些降解掉的脂质体更有可能**免疫反应。Peer一直在开发一系列新的脂质体,并授权给他的公司NeoVac,这些脂质体显示出更高的生物降解性和更低的免疫原性,以及其他特征。“我们相信,含有较少的免疫原性的脂质体将更适合于**性LNP药物的开发。并且有助于LNP更有效地递送载荷”。目前阻碍递送效率的障碍之一是:当LNP被细胞吸收后,没有完全释放到细胞质前,它们往往会被困在内涵体中。“改善的内体逃逸对于未来几代LNP来说,将是一件大事,因为目前的LNP估计只有不到5%,能完成内涵体逃逸,” Whitehead说。更多的逃逸将允许使用较低剂量的LNP,从而减少可能的细胞毒性副作用。
扩大LNP用途的另一个关键挑战是找到可以使它们到达身体不同部位的方法。LNPs天然靶向到肝脏,但对于靶向基因**等应用,有必要将它们引导到其他**,如肺,肾或大脑。“有一种内在的需要,即绕过每个**特有的障碍,”Eygeris说。这意味着需要防止LNP在肝脏的积聚的同时,也要将LNP引导到特定位置。例如,他们需要穿过血脑屏障才能在大脑中发挥作用。
究竟如何更好地将LNP引导到其所需的靶点,并不是一个简单的问题。“不同的人正在尝试不同的方式,没有人有明确的答案,”Mui说。一些小组正在研究LNP中的脂质体如何影响对不同**的靶向,而另一些研究小组正在探索,将靶向配体添加到LNP表面以帮助它们与特定细胞结合的作用。
Eygeris说,寻找新的LNP是一个非常活跃的研究领域。“这就是每个人现在都在做的事情,”她说。“如果你有一些东西或方法能够绕过肝脏进入任何其他**,如肺或脾脏,那么这就会**增加你的**潜力。
与此同时,Peer还专注于提高纳米颗粒的热稳定性。**交付的LNP-mRNA COVID-19疫苗的一个障碍是:需要将其储存在非常低的温度下;而热稳定好的LNPs有可能保持在室温下。Peer的小组仍在测试他们开发的热稳定脂质体,他希望他们能够将mRNA疫苗提供给更多国家,特别是在南半球。“热稳定配方对于改变mRNA疫苗和**方法的格局至关重要,不管你有没有冰柜,你都可以获得LNP-mRNA疫苗”Peer说。
Peer对大流行之后,基于LNP的**持乐观态度,尽管他指出还有很多工作要做。“但是,在****期间,我们学到了很多东西,现在是时候进入下一个级别了。”他说。