一、 详细信息
8款抗体新药的制剂处方详细信息如下。
1.Evkeeza
Evkeeza为靶向ANGPTL3的降血脂FIC新药,由再生元研发。
Evinacumab-dgnb是一种血管生成素样蛋白3 (ANGPTL3)抑制剂单克隆抗体(IgG4同型),通过重组DNA技术在中国仓鼠卵巢(CHO)
细胞悬浮培养获得,分子量约为146 kDa。
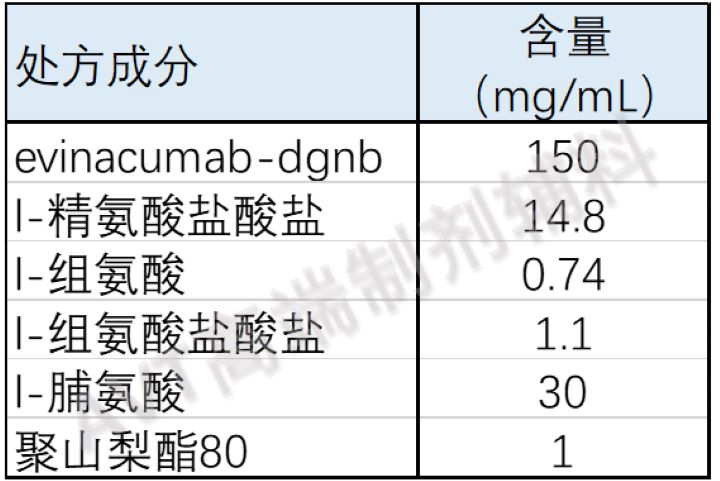
EVKEEZA (evinacumab-dgnb)注射剂是一种无菌、无防腐剂的静脉注射用溶液。溶液清澈至微乳白色,无色至淡黄色,无可见颗粒。
每瓶含有345mg/2.3 mL或1200mg/8mL溶液,pH值为6。
制剂处方信息如下:
2.Jemperli
Dostarlimab为FDA批准的第4款PD-1抗体,最初由Anaptysbio研发,为首个动物细胞展示平台技术来源的抗体药物。药明生物为Dostarlimab提供CMO服务。
Dostarlimab-gxly是一种PD-1阻断IgG4人源化单克隆抗体。Dostarlimab-gxly在中国仓鼠卵巢细胞中产生,分子量约为144 kDa。
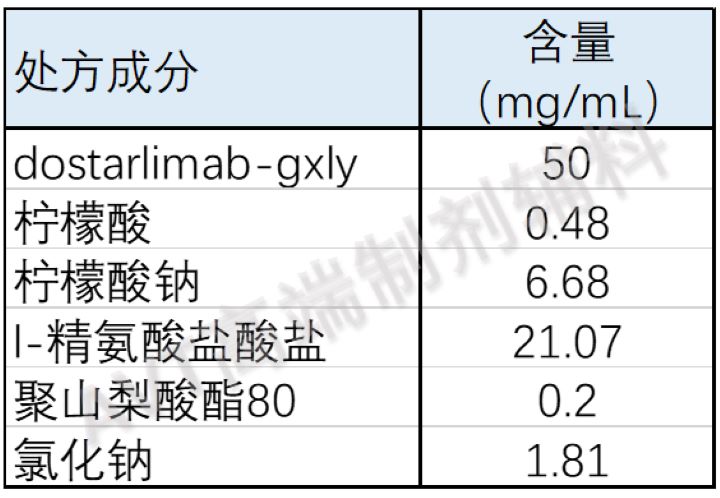
Jemperli(dostarlimab-gxly)是一种无菌、透明至微乳白色、无色至黄色的溶液,基本上没有可见颗粒,每瓶10mL。
制剂处方信息如下:
3.Zynlonta
Zynlonta是首个CD19 ADC新药,由ADC Therapeutics研发,采用PBD毒素和SG3249连接子。
Loncastuximab tesirine-lpyl是一种CD19指向的抗体和烷基化剂偶联物,由人源化IgG1 kappa单克隆抗体通过蛋白酶可裂解的缬氨酸
-丙氨酸连接子偶联到吡罗苯二氮(PBD)二聚体细胞毒性烷基化剂SG3199。连接到连接器上的SG3199被称为SG3249,也称为tesirine。
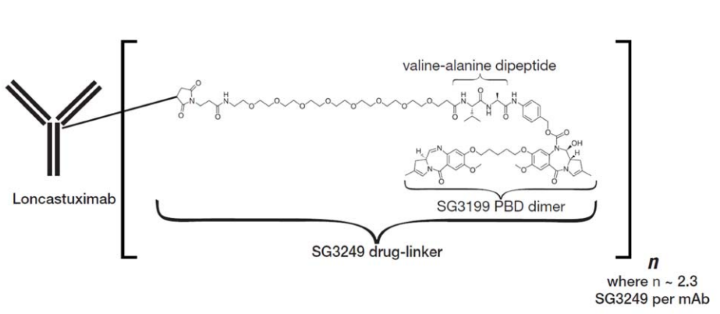
(https://www.accessdata.fda.gov/drugsatfda_docs/label/2021/761196s000lbl.pdf)
Loncastuximab tesirine-lpyl的分子量约为151kDa。每个抗体分子上平均附着2.3个SG3249分子。Loncastuximab tesirine-lpyl是抗体和小分子成分通过化学偶联形成的。其中抗体由哺乳动物(中国仓鼠卵巢)细胞产生,小分子成分通过化学合成产生。
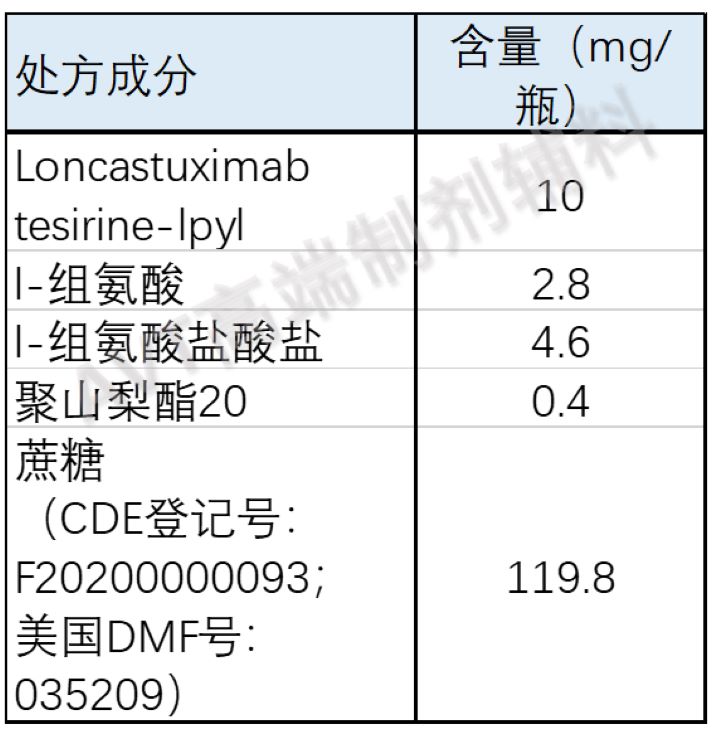
ZYNLONTA (loncastuximab tesirine-lpyl)是一种无菌,白色至米白色,不含防腐剂的冻干粉末,外观像蛋糕,在重溶和稀释后用于静脉注射。每个单剂量瓶用2.2mL无菌注射用水复配后,最终浓度为5mg/mL, pH约6.0。
制剂处方信息如下:
4.Rybrevant
Rybrevant为FDA批准第3款双抗,用于治疗EGFR20外显子插入突变的NSCLC。
Amivantamab-vmjw是一种低聚焦的基于人免疫球蛋白g1的双特异性抗体,针对EGF和MET受体,由哺乳动物(中国仓鼠卵巢CHO)细胞使用重组DNA技术生产,分子量约为148kDa。
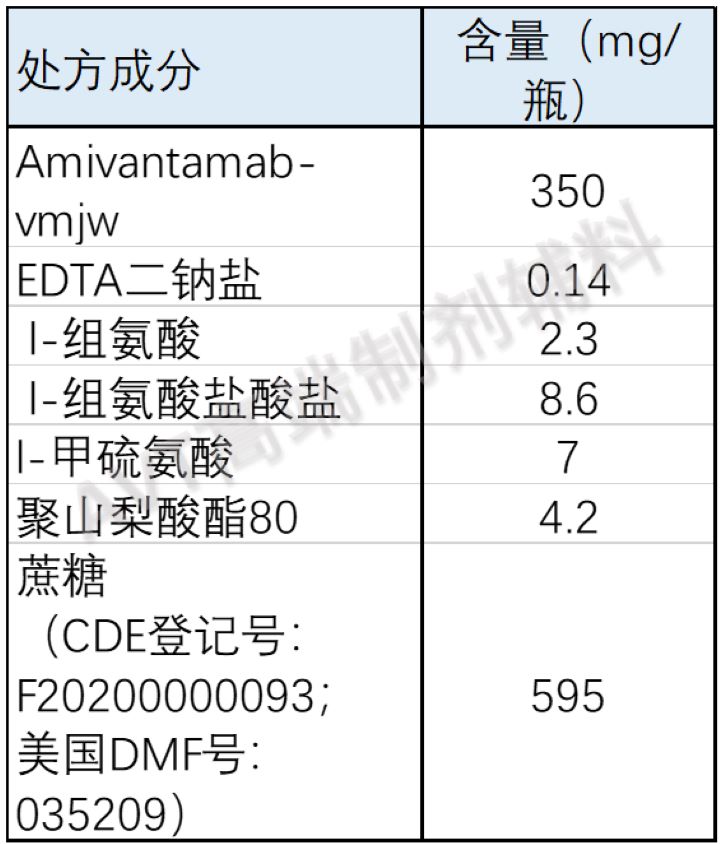
Rybrevant (amivantamab-vmjw)静脉输液注射剂是一种无菌、无防腐剂、无色至淡黄色的单剂量瓶溶液。pH值为5.7。
制剂处方信息如下:
5. Aduhelm
Aduhelm为Aβ单抗,是FDA2003年以来批准的首个阿尔茨海默症药物。但临床疗效存在争议,受到医生的普遍抵制,2021年前三季度销售额仅200万美元,其中三季度销售额仅30万美元。
Aducanumab-avwa是一种重组人免疫球蛋白γ 1 (IgG1)单克隆抗体,针对的是聚集的可溶性和不溶性β淀粉样蛋白,在中国仓鼠卵巢细胞系中表达,分子量约为146 kDa。
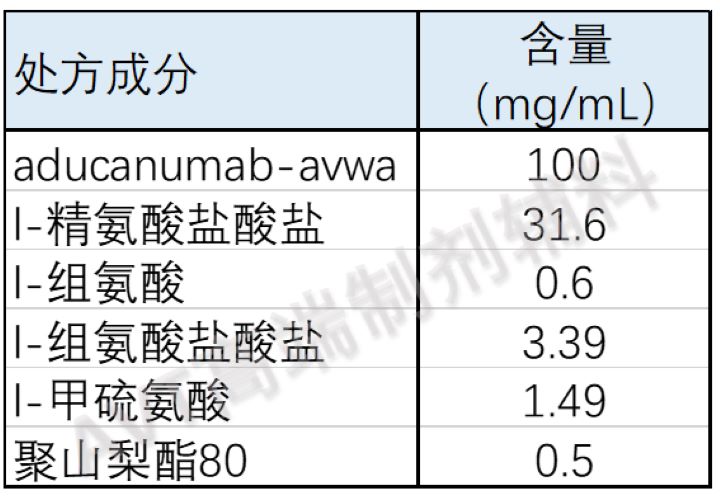
Aduhelm (aducanumab-avwa)注射剂是一种无防腐剂,无菌,透明至乳白色,无色至黄色的溶液,稀释后供静脉滴注,浓度为170mg/1.7mL或300mg/3mL(100 mg/mL),pH约为5.5。
制剂处方信息如下:
6.Saphnelo
Anifrolumab为贝利木单抗之后10年来第一款狼疮新药,其开发之路颇为坎坷, 2019年,Anifrolumab的第2项三期临床宣告成功。国内方面,智翔金泰和荃信生物的IFNAR1抗体已经申报临床。
anfrolumab-fnia是一种I型干扰素(IFN)受体拮抗剂,免疫球蛋白G1κ (IgG1κ)单克隆抗体,通过重组DNA技术在小鼠骨髓瘤细胞(NS0)中产生,分子量约为148kDa。
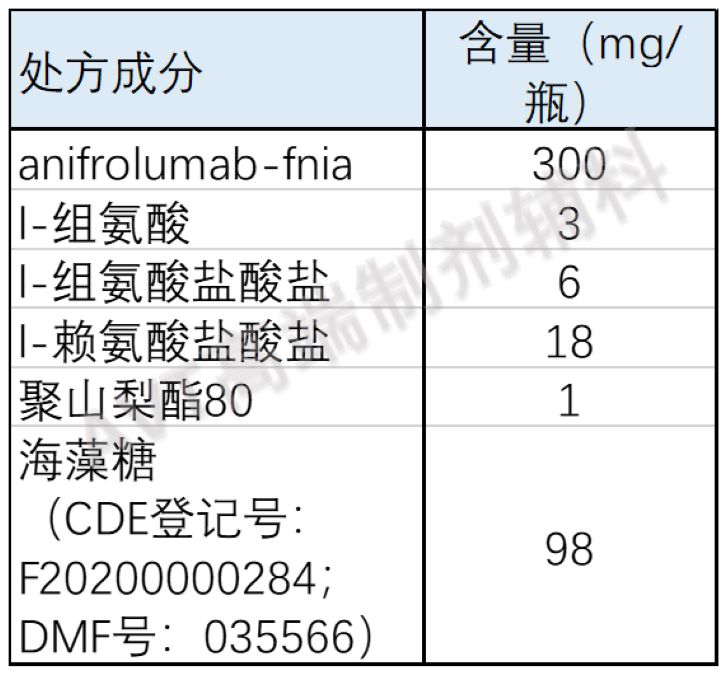
Saphnelo (anifrolumab-fnia)注射液是一种无菌,无防腐剂,透明至乳白色,无色至微黄色,供静脉注射使用的溶液。SAPHNELO含有的anfrolumab-fnia浓度为150mg/mL,单剂量瓶,每瓶2mL。pH为5.9。
制剂处方信息如下:
7.Tivdak
Tisotumab Vedotin为靶向组织因子(TF)的FIC药物,二期临床表现出优异的疗效。国内方面,乐普生物研发了国内首个TF ADC,今年2月获得FDA批准临床,6月在国内递交临床试验申请。
Tisotumab vedotin-tftv是一种组织因子(TF)定向抗体药物偶联物(ADC),由人抗TF IgG1-kappa抗体通过蛋白酶可切割vc(缬氨酸-瓜氨酸)连接子偶联到微管破坏剂单甲基auristatin E (MMAE)。该单克隆抗体是在一种哺乳动物细胞(中国仓鼠卵巢细胞)中产生的。MMAE和连接剂通过化学合成获得。每个单克隆抗体分子平均携带4个MMAE分子。Tisotumab vedotin-tftv的分子量约为153 kDa。其化学结构如下:

(https://www.accessdata.fda.gov/drugsatfda_docs/label/2021/761208Orig1s000lbledt.pdf)
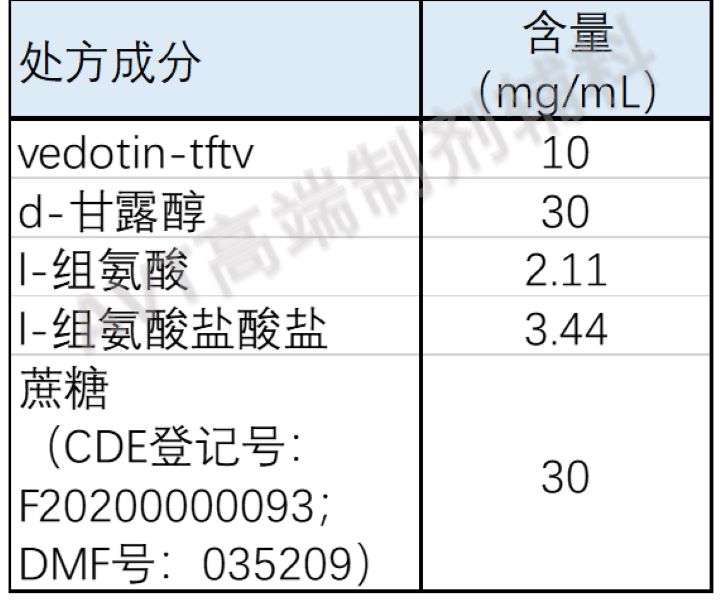
Tivdak (tisotumab vedotin-tftv)供注射用,为无菌、无防腐剂、白色或灰白色的冻干饼或粉末,单剂量瓶,稀释后用于输注。用4mL无菌注射用水复配后,制备出含10mg/mL tisotumab vedotin-tftv的清澈至微乳白色、无色至棕黄色溶液,pH为6.0。
制剂处方信息如下:
8.Tezspire
Tezspire的研发也颇为曲折,2020年11月10日,阿斯利康宣布TSLP抗体Tezepelumab的三期临床NAVIGATOR获得成功。2020年12月22日,阿斯利康宣布Tezepelumab的第二项三期临床SOURCE失败。这两项三期临床的主要终点标准不同,SOURCE的主要终点为口服激素减少的剂量。NAVIGATOR的主要终点为AAER的下降。虽然不能减少激素用量,但Tezepelumab降低AAER的效果还是非常显著的,因此顺利获得FDA批准上市。
Tezepelumab-ekko是一种胸腺基质淋巴细胞生成素(TSLP)阻断剂,是一种利用重组DNA技术在中国仓鼠卵巢(CHO)细胞中产生的人单克隆抗体免疫球蛋白G2λ (IgG2λ)。Tezepelumab-ekko的分子量约为147 kDa。
Tezspire (tezepelumab-ekko)注射剂是一种无菌,无防腐剂,透明到乳白色,无色到淡黄色的溶液,用于皮下注射,以单剂量瓶或单剂量预充注射器的形式提供使用,每个单剂量瓶或预充注射器包含1.91 mL溶液,pH为5.2。
制剂处方信息如下:

三、总结
抗体蛋白在抗体药物中担任着至关重要的角色,如同冲锋在前的勇士。然而,与之同样重要的还有制剂中的各类辅料,它们如同稳固的后勤支援,确保抗体药物在整个生命周期内都保持稳定、高效。
正如古人的智慧所说:“兵马未动,粮草先行。”如果没有充足的后勤保障,即便是最精锐的战士也难以持续发挥其战斗力。同样,一个优质的制剂处方就像是一个与抗体药物完美配合的后勤体系,对确保药物从生产到使用的每一步都发挥出最佳效果起到了至关重要的作用。
在开发蛋白制剂时,一个重大的挑战是如何基于对蛋白分子稳定性的深入理解,来合理地设计、优化剂型和含量。同时,研究不同的药物辅料对蛋白稳定性的影响也是一项艰巨的任务。由于药用辅料的多样性,全面评估各种不同的组合和浓度不仅成本高昂,而且在时间上也极为有限。
由于临床研究和时间的压力,制剂开发者常常需要尽快找到稳定的制剂处方用于临床试验。因此,借鉴和学习成熟制剂处方的方法为制剂开发者提供了快速选择辅料并确定处方的有效途径。
近年来,全球抗体新药的发展势头迅猛。抗体药物的研发呈现出多样化趋势,包括ADC药物、单/双/多特异性抗体和纳米抗体等。这些创新药物主要针对抗肿瘤和抗风湿类免疫疾病领域,但也在其他领域逐渐展现出其独特的疗效。
为了更好地推动相关制剂的研发和工艺优化,本文将重点分析2021年FDA批准上市的8款抗体新药的处方信息。希望通过这些分析为制剂研发人员和工艺工程师提供有价值的参考与帮助。
如果您对本文有任何疑问或建议,或者需要关于高端药用辅料的专业咨询和优质服务,请随时与我们联系。艾伟拓始终致力于为广大客户提供最优质的服务和支持!
艾伟拓长期稳定供应注射级蔗糖海藻糖,超低内毒素,符合各国药典标准,助力产品中外申报!